Uma solução contendo CO2(aq) e HCO3(-) em equilíbrio define um pH igual a 5,6 para a água pluvial. Este é considerado o pH limite, abaixo do qual se qualifica uma chuva como sendo "ácida". Aqui não estão sendo levados em conta outros componentes químicos estranhos a composição normal do ar atmosférico, que também determinam condições de chuva ácida, tais como óxidos de enxofre e de nitrogênio. Para um melhor entendimento do conceito de pH, observe o quadro seguinte.
Índice pH
O índice pH mede a acidez ou a basicidade alcalinidade uma solução aquosa, normalmente variando entre os limites de 0 a 14. O valor "0" eqüivale a uma forte acidez e o "14" a uma forte basicidade. Se a solução não for nem ácida nem básica, o seu pH será igual a 7. A acidez aumenta a partir do pH 7 (excluindo este para valores mais baixos e a basicidade aumenta no sentido dos valores acima do pH 7.
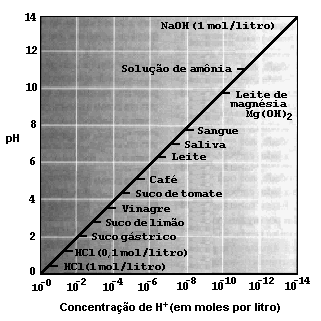
Figura extraída do livro Planeta Azul
O fato de a chuva ser ácida traz certos efeitos, por exemplo, a erosão química de monumentos. Normalmente qualquer material exposto ao ambiente e sob a ação de chuvas, ventos, organismos vivos etc. sofre uma degradação denominada "intemperismo". Na construção de edifícios, pisos, monumentos, estátuas etc., utilizam-se rochas, tais como os calcários e os mármores , que tem como componente quimico principal o carbonato de cálcio (CaCO3), em geral sob a forma cristalina de um mineral chamado "calcita". Quando sujeito a ação das chuvas, esse material se desagrega, ocasionando a destruição ou danificação de fachadas de prédios, degraus de escadarias e pisos, além da perda do valor estético de monumentos, estátuas e similares. O processo de ataque da chuva ácida deriva da reação química entre o carbonato de cálcio e o ácido carbônico, levando a formação de bicarbonato de cálcio (Ca(HCO3)2) que é solúvel na água, ao passo que o carbonato não o é.

Figura extraída do livro Planeta Azul
Outro efeito das chuvas normalmente ácidas é a formação de cavernas. Em certas regiões, o sub-solo compõe-se de rochas calcárias, podendo ocorrer infiltrações da água das chuvas, que penetra nos corpos rochosos, causando a sua dissolução na forma de bicarbonato de cálcio. Ao se introduzir por juntas e poros dessas rochas, a água vai alargando os vazios, abrindo canais e, às vezes, cavando grandes espaços ocos (cavernas). Tais cavernas apresentam sob a forma de corredores e salões subterrâneos, alguns de grande extensão. No caso de o teto dessas cavernas desabar, há o afundamento do terreno sobrejacente e a formação de depressões afuniladas que são chamadas "dolinas". Eventualmente as depressões acumulam água, dando origem a lagoas mais ou menos circulares. Já os desabamentos em áreas habitadas provocam a destruição de edificios e vias públicas, como já aconteceu, na década de 80, em cidade da Grande São Paulo.
Nas cavernas calcárias, ocorre a infiltração das águas superficiais ou de lençóis de água subterrânea, carregadas de bicarbonato de cálcio, que afloram no teto, de onde gotejam. Tais gotas, ao serem expostas ao ar, perdem o gás carbônico dissolvido; assim, o bicarbonato de cálcio volta a forma de carbonato, que por ser insolúvel, precipita-se, formando cristais de calcita. No decorrer dos tempos, esses cristais fundem-se em grandes massas pendentes do teto das cavernas; trata-se das estalactitas, que assumem as mais variadas formas (colunas, cortinas, tubas de orgão, figuras de animais etc.). Por processo semelhante, as gotas de água carregadas de bicarbonato que caem no solo formam as estalagmitas. São essas formações que dão extraordináriaria beleza às grutas calcárias, transformando-as em atrações turísticas. Em condições especiais, os cristais de calcita precipitam-se dentro de poças d'água, originando espetaculares estruturas globulares chamadas "pérolas das cavernas". As águas de infiltração que geram as cavernas calcárias podem ser drenadas por cursos d'água subterrâneos, que eventualmente afloram nas proximidades dessas formações geológicas. É de se esperar que o interior das cavernas contenha ar com um alto teor de gás carbônico, que se acumula nas partes baixas (o CO2 é mais denso que o ar), especialmente junto ao solo. Esse fato representa um perigo para os exploradores de cavernas e, em alguns casos, chega a impedir a entrada de pequenos animais, que são sufocados por estarem com as narinas mergulhadas no gás carbônico acumulado próximo ao solo. Um exemplo desse tipo de fenômeno da Gruta do Cão, localizada na Itália.
Há cavernas calcárias em muitas regiões do Brasil, sendo mais famosas as da região da Lagoa Santa, em Minas Gerais: Lapinha, Maquiné, Lapa Nova, Lapa Vermelha e São João del Rei (a Lagoa Santa, por sua vez, que tem forma circular, resultou do desabamento do teto de uma caverna, formando uma dolina que for preenchida por águas subterrâneas). Também bastante conhecidas, as formações do Vale do Ribeira de lguape, em São Paulo, constituem o maior conjunto de cavernas calcárias no pais; entre elas destaca-se a Caverna do Diabo, ponto turístico da região. Existem cavernas deste tipo em outras regiões do Brasil, como a que abriga o Santuário do Bom Jesus da Lapa, na Bahia, e as do vale do Rio Salitre, no estado do Ceará. No âmbito mundial, as mais famosas são as enormes Cavernas de Carlsbad, localizadas no sudoeste do estado do Novo México, nos Estados Unidos.
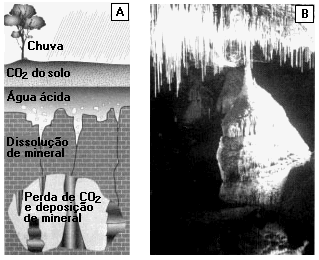
Figura extraída do livro Planeta
Azul