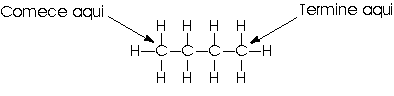
Agora podemos voltar ao metano (CH4), etano (C2H6) e propano (C3H8) para ver um pouco mais detalhadamente como o propano difere dos outros dois alcanos. Nós vimos que trocando qualquer um dos quatro hidrogênios equivalentes do metano por um grupo metílico, obtemos a estrutura da molécula do etano. Similarmente, trocando qualquer um dos seis hidrogênios metílicos equivalentes do etano por um grupo metílico obtemos a estrutura da molécula do propano.
Mas o resultado não é o mesmo quando o composto é o propano. Isso porque ele contém dois tipos diferentes de hidrogênio, dois secundários e seis primários, importando agora qual dos hidrogênios é substituído. Substituindo um dos seis hidrogênios primários por um grupo metílico obtemos o CH3CH2CH2CH3, alcano de fórmula molecular C4H10, chamado de butano. Trocando um dos dois hidrogênios secundários por um grupo metílico obtemos o HC(CH3)3, que é conhecido como isobutano.
Como os nomes já evidenciam, butano e isobutano são compostos diferentes. Eles possuem estruturas moleculares diferentes com diferentes números de carbono e hidrogênios primários, secundários e terciários, além de diferentes propriedades. O butano, por exemplo, entra em ebulição a -0,5° C, enquanto o isobutano a -11,6° C. Embora sejam compostos diferentes, eles possuem a mesma fórmula molecular, C4H10. Compostos diferentes que compartilham a mesma fórmula molecular são conhecidos como isômeros, uma palavra derivada das palavras gregas isos, que quer dizer o mesmo, e meros que quer dizer uma parte. Neste sentido, os isômeros possuem a mesma fórmula molecular. Portanto, o butano e o isobutano fornecem um ótimo exemplo de isomeria.
O isobutano e o butano também servem
como exemplo de compostos com cadeia reta e ramificada. Olhemos primeiramente
para a cadeia reta do butano. Para compreender porque sua cadeia carbônica
é chamada de reta, imagine que você está numa das pontas
da cadeia e comece a andar por cima dela até a outra ponta.

Você poderá atravessar os dois grupos metilênicos até alcançar a outra parte da cadeia em linha reta. Certamente você não encontrou, qualquer tipo de ramificação ao longo da cadeia. Por isso é que a cadeia carbônica do butano é dita reta.
Se você repetir o mesmo procedimento
para o isobutano, logo perceberá a existência de uma ramificação
no seu caminho.
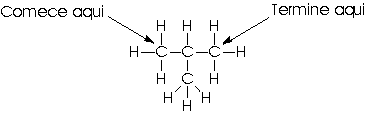
No carbono terciário você deverá decidir em qual dos dois grupos metílicos restantes você caminhará. É por isso que a cadeia carbônica do isobutano é chamada de ramificada.
A grande variedade estrutural dos compostos
orgânicos resulta, em parte, devido às possibilidades de isomeria.
Quanto maior for o número de carbonos presentes no alcano ou em
qualquer outro tipo de composto orgânico, maior a variedade de estruturas
covalentes que podem ser formadas e maior o número de isômeros
possíveis. A isomeria geralmente não é possível
em moléculas pequenas, constituídas de poucos átomos.
Como vimos, somente uma estrutura é possível para o metano
(um carbono e quatro hidrogênios), uma para o etano (dois carbonos,
seis hidrogênios) e uma para o propano (três carbonos e oito
hidrogênios). O butano, contudo, com seus quatro carbonos e dez hidrogênios
pode ser arranjado em duas moléculas diferentes, butano e isobutano.
À medida que o número de átomos na molécula
aumenta, aumenta também a capacidade de formar isômeros, e
os nomes que devemos usar para identificar cada um deles devem ser diferentes.
Mais para a frente, você aprenderá como dar nome a cada um
dos alcanos de cadeia reta e aos de cadeia ramificada.
 |
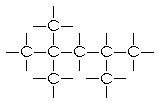 |
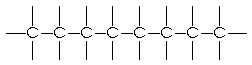
| Fig. Os compostos n-octano e i-octano são isômeros porque possuem fórmulas moleculares idênticas. | |