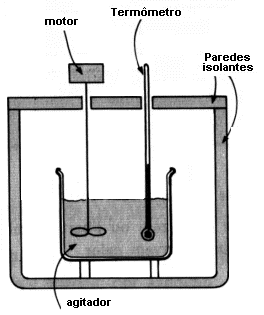
O calor absorvido ou liberado
em uma reação química pode ser medido por aparelhos
denominados calorímetros, que variam em detalhes e são
adaptados para cada tipo de reação que se quer medir o calor.

Nesse aparelho, mede-se a variação de temperatura de uma massa conhecida de água, na qual está mergulhado o recipiente de reação. Para as medidas serem precisas, o sistema deve ser isolado ao máximo para evitar trocas de calor com o ambiente.
A determinação do calor liberado ou absorvido numa reação química é feita através da expressão:
sendo m = massa de água presente no aparelho, em gramas; c = calor específico da água, em cal/g.° C; D T = variação da temperatura da massa de água, em ° C.
A rigor, deve-se considerar também a capacidade térmica do calorímetro.
Na equação anterior, o calor envolvido foi medido em calorias (cal). Uma caloria é a quantidade de calor necessária para aquecer um grama de água de 14,5° C a 15,5° C.
No Sistema Internacional de Unidades (S. I.), a quantidade de calor é expressa em joules (J), sendo que 1 cal = 4,18 J.
Exercícios Resolvidos e Exercícios Propostos